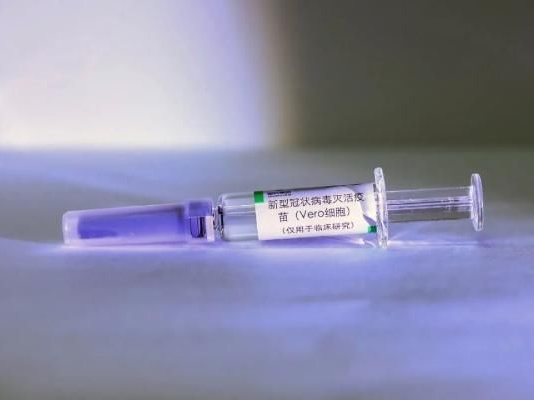
康希诺生物的重组新冠疫苗。
3月22日,康希诺生物(688185.SH,6185.HK)发布公告称,公司的重组新冠疫苗(5型腺病毒载体)克威莎获得匈牙利国家药品与营养研究院的紧急使用授权,这也是康希诺首次获得欧盟成员国的批准。
康希诺生物新冠疫苗是与军事科学院陈薇院士团队联合研发,今年2月25日获得国家药品监督管理局批准在国内附条件上市,也是国内首个获批的腺病毒载体新冠疫苗。在国外,该疫苗已获得巴基斯坦、墨西哥的紧急使用授权。
康希诺生物新冠疫苗系单针免疫,根据其公开的三期临床试验设计,该疫苗推荐的接种年龄为是18岁及以上成年人,未设年龄上限。
在疫苗有效性上,澎湃新闻记者此前从康希诺生物方面获悉,目前该疫苗的全球三期临床数据表明,单针接种疫苗28天后,康希诺生物新冠疫苗总体保护效力为65.28%。另外,境内I期临床试验部分受试者进行了6个月加强免疫研究,结果表明6个月加强免疫后抗体水平升高10倍或以上。
值得关注的是,康希诺生物新冠疫苗与近期深陷血栓等不良反应风波的阿斯利康/牛津新冠疫苗同属于腺病毒载体技术路线。此前有超过10个欧盟国家暂停接种阿斯利康/牛津新冠疫苗,随着欧洲药品管理局3月18日宣布阿斯利康/牛津新冠疫苗“安全有效”的初步调查结果后,法国、德国等国家相继恢复接种该疫苗。
不过,阿斯利康/牛津新冠疫苗导致血栓的质疑并未完全消失。海外网援引《华尔街日报》3月19日消息称,德国和挪威的科学家表示,他们已确定阿斯利康疫苗与血栓报告之间的潜在联系。两个研究小组独立发现该疫苗会引起自身免疫反应,引起抗体形成,它们进而再与血小板发生相互作用,导致大脑中产生血栓。
对同属于腺病毒载体新冠疫苗的克威莎的安全性,康希诺生物向澎湃新闻记者强调,根据全球多中心三期临床试验中期数据表明,未发生任何与疫苗相关的严重不良反应,综合其保护效力的数据来看,疫苗具有良好的安全性和有效性,尤其在老年人群中的不良反应发生率更低。
(原题《首次获得欧盟成员批准!康希诺新冠疫苗获匈牙利紧急使用权》)
编辑 董雯静 审读 韩绍俊 审核 王雯 曹亮