3月4日,读特记者从广东省药品监督管理局官网了解到,飞利浦金科威(深圳)实业有限公司召回两批次医疗器械,分别为病人监护仪及心电电缆。据了解,病人监护仪生产数量为9303台,其中,在中国的销售数量为7720台;心电电缆生产数量为46339条,在中国的销售数量为7650条。
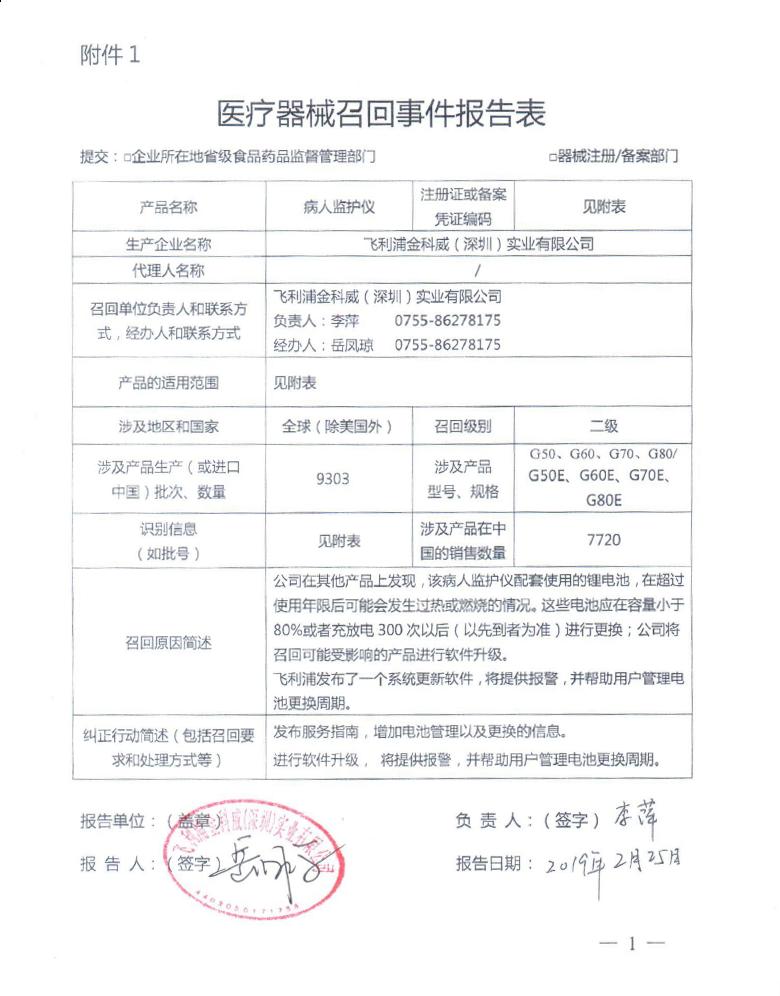
据报告,病人监护仪召回原因为部分仪器配套使用的锂电池,在超过使用年限后可能会发生过热或燃烧的情况。飞利浦金科威(深圳)实业有限公司对其生产的病人监护仪主动召回。召回级别为二级。公司将召回可能受影响的产品进行软件升级,系统将提供报警,并帮助用户管理电池更换周期。涉及产品的型号、规格及批次等详细信息见下表↓↓
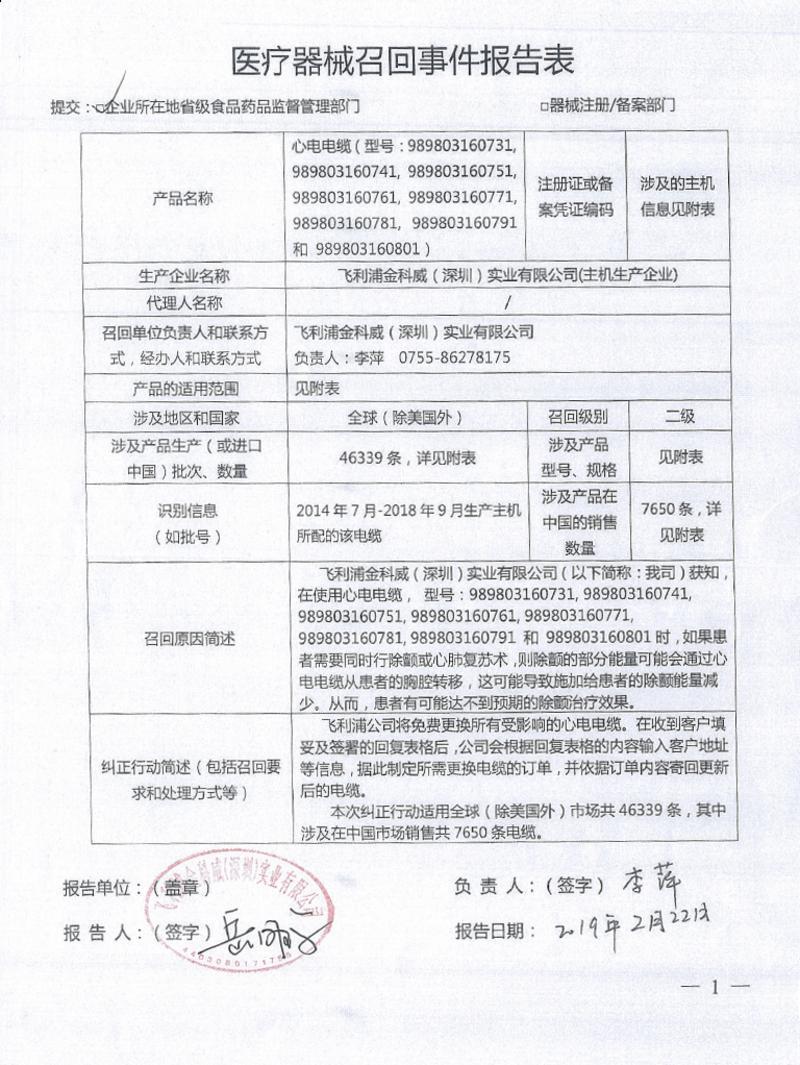
另据报告,心电电缆召回原因为在使用型号为:989803160731、989803160741、989803160751、989803160761、989803160771、989803160781、989803160791、989803160801的心电电缆时,如果患者需要同时进行除颤或心肺复苏术,则除颤的部分能量可能会通过心电电缆从患者的胸腔转移,这可能导致施加给患者的除颤能量减少,从而达不到预期的除颤治疗效果。飞利浦金科威(深圳)实业有限公司对其生产的心电电缆主动召回,将免费更换所有受影响的心电电缆。
(晶报供稿)
编辑 曹阳