
北京时间10月4日下午5点45分,瑞典皇家科学院秘书长戈兰·K·汉森宣布,将2017年诺贝尔化学奖授予瑞士洛桑大学的杰克·豆布切特(Jacques Dubochet)、美国哥伦比亚大学乔基姆·弗兰克(Joachim Frank)和英国剑桥大学理查德·亨德森(Richard Henderson ),表彰他们“研发出能确定溶液中生物分子高分辨率结构的冷冻电子显微镜”。他们三人将分享900万瑞典克朗(约734万人民币)奖金。
正是因为他们的努力,人类才得以用极高的分辨率看清重要的生物分子。

杰克·豆布切,1942年生于瑞士,1973年博士毕业于日内瓦大学和瑞士巴塞尔大学,瑞士洛桑大学生物物理学荣誉教授。迪波什博士领导的小组开发出真正成熟可用的快速投入冷冻制样技术制作不形成冰晶体的玻璃态冰包埋样品,随着冷台技术的开发,冷冻电镜技术正式推广开来。

乔基姆·弗兰克,德裔生物物理学家,现为哥伦比亚大学教授。他因发明单粒子冷冻电镜(cryo-electron microscopy)而闻名,此外他对细菌和真核生物的核糖体结构和功能研究做出重要贡献。弗兰克2006年入选为美国艺术与科学、美国国家科学院两院院士。2014年获得本杰明·富兰克林生命科学奖。

理查德·亨德森,1945年生于苏格兰爱丁堡,分子生物学家和生物物理学家,他是电子显微镜领域的开创者之一。1975年,他与Nigel Unwin通过电子显微镜研究膜蛋白、细菌视紫红质,并由此揭示出膜蛋白具有良好的机构,可以发生α-螺旋。近年来,亨德森将注意力集中在单粒子电子显微镜上,即用冷冻电镜确定蛋白质的原子分辨率模型。
有人说,一图胜千言,科学研究也是如此。在历史长河里,许多重要的发现都是基于人类的观察。然而,在一些技术所不能及的领域,获取图片就成了一桩异常困难的事,也阻碍了人类对自然的进一步理解。在这三名科学家的努力下,冷冻电镜应运而生。科学家们能将生物分子“冻起来”,并以前所未有的方式对它们进行观察。
长期以来,人们认为电子显微镜不适合观察生物分子,因为强大的电子束会破坏生物材料。但是在1990年,Richard Henderson教授成功地使用电子显微镜显示蛋白质的三维图像,达到原子级分辨率。这一突破性成果证明了用电子显微镜进行生物分子成像的潜力。
Joachim Frank教授让这项技术变得有普遍应用价值。在1975年到1986年之间,他研发出了一种图像处理方法,能通过分析和合并电子显微镜的模糊二维图像,揭示一个清晰的三维结构。
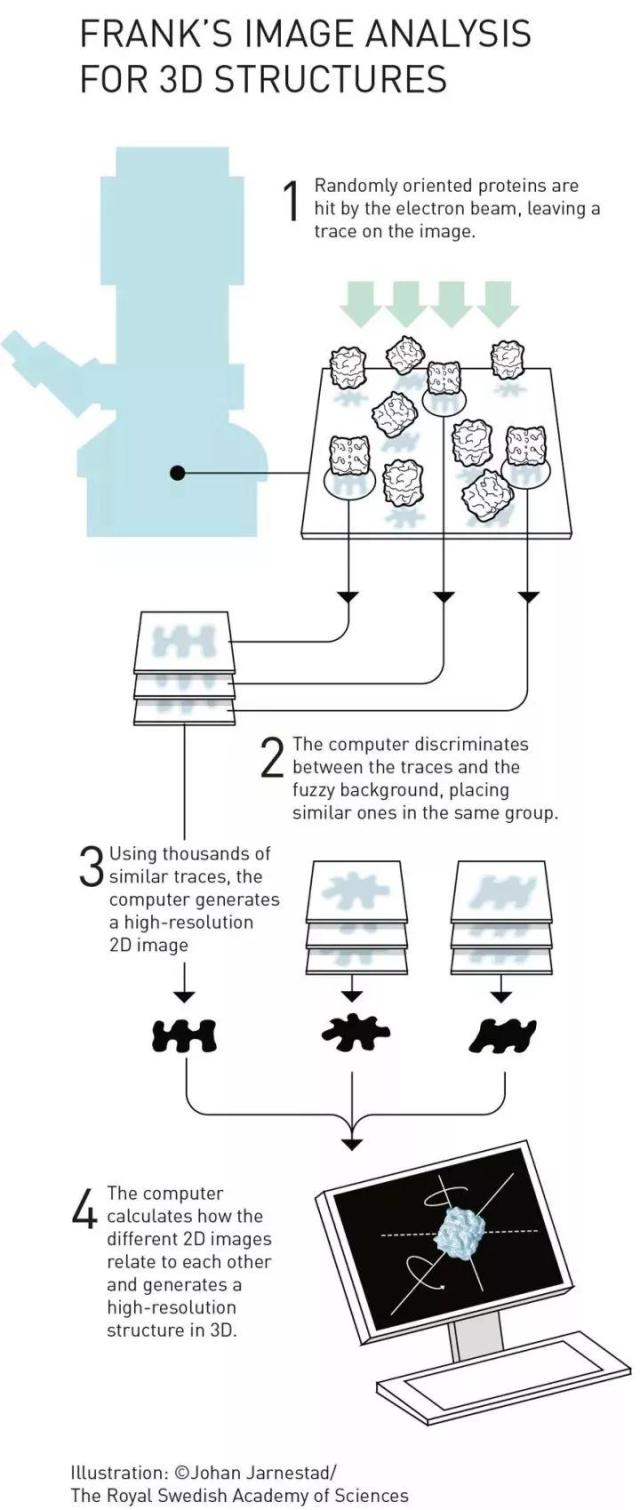
↑Frank教授降低了图片分析的门槛
Jacques Dubochet教授将水添加到了电子显微镜中。液态水在电子显微镜的真空环境下中蒸发,从而瓦解了生物分子。在上世纪80年代初,Dubochet教授成功的把水进行了玻璃化(vitrifying water)——他把水冷却得如此迅速,以至于水可以在生物样本周围凝固。这样一来,即使在真空环境中,生物分子也能保持其自然形状。
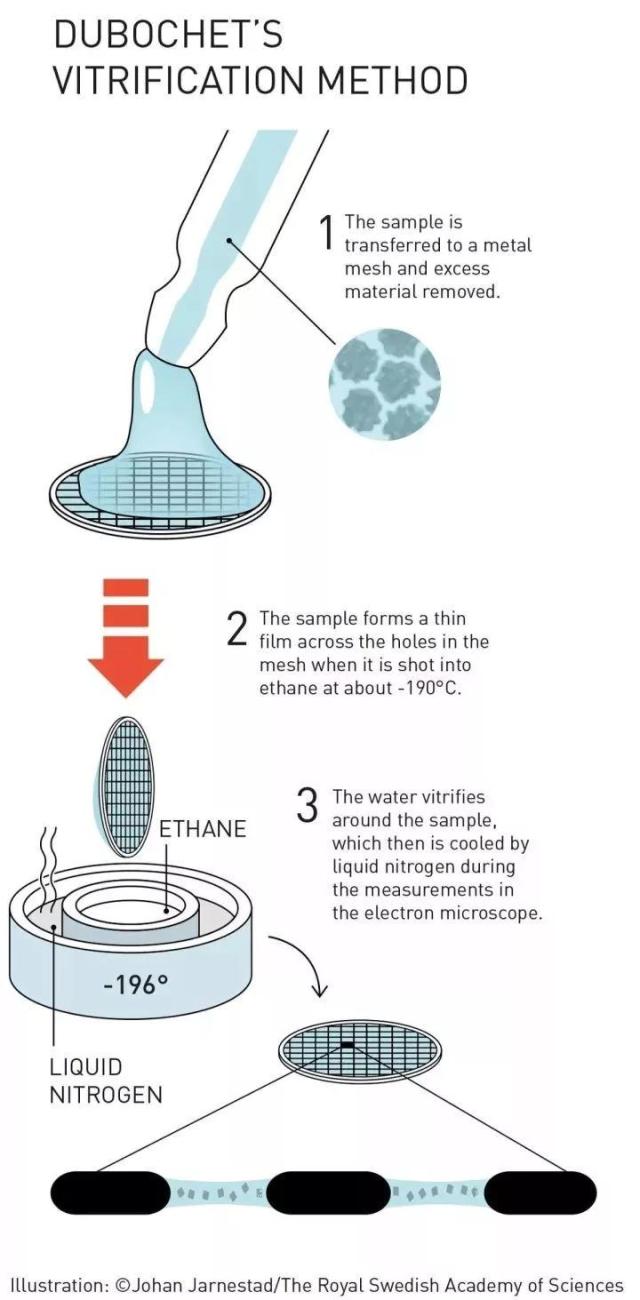
↑Dubochet教授的创新设想
随后,冷冻电镜的每一部分得到了进一步的优化。2013年,这项技术终于臻于成熟,让科学家们能轻松地看清生物分子的结构。在过去的几年里,这一领域迎来了井喷。从抗体蛋白到剪接体结构,一个全新的世界出现在我们面前。
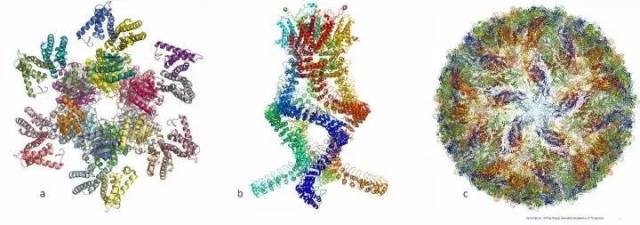
↑生物世界从未变得如此清晰
冷冻电镜的诞生让我们得以畅想未来。
我们不需要再辛辛苦苦地预测蛋白质的构象,只要拍一张“照片”就能知道蛋白质乃至蛋白质复合体相对真实的结构。譬如下面这张图,就是一个复杂的蛋白复合体的精细三维结构图,分辨率可达20 ?——它发表在近期的《自然-通讯》(Nature Communications)杂志上。
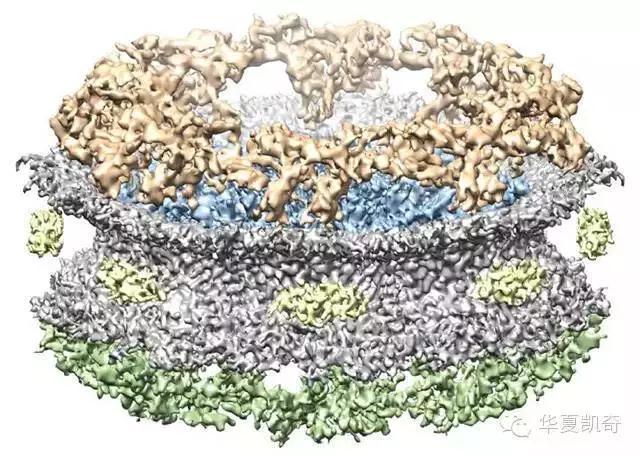
↑图中所拍摄的是核孔复合体
图中所拍摄的是核孔复合体(Nuclear Pore Complexes,NPCs),生物体内最复杂的蛋白质复合体之一,它由多达三十多种不同的蛋白质共同构建而成,依赖传统技术显然无法得到它的准确构象。不过通过冷冻电镜技术,研究人员成功还原了该复合体的精细结构。
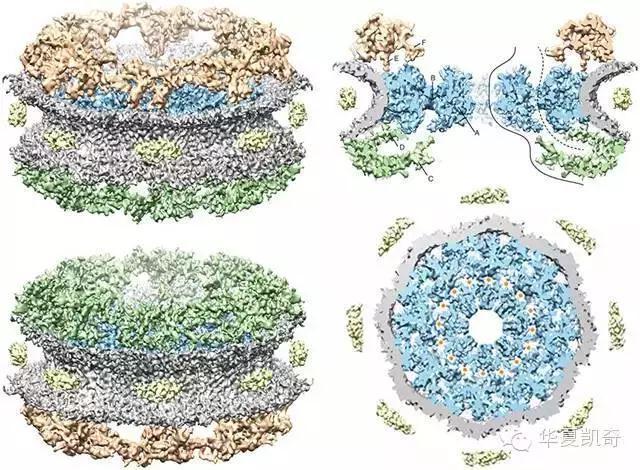
↑核孔复合体不同角度的影像
也许有一天,所有生命的复杂结构都能以原子的清晰度展现在人类面前。我们相信,在那一刻,人类对生命的理解会上升到一个全新的高度,带来生物化学的新纪元。今日授予这三名科学家的诺贝尔化学奖,也是对他们突破性贡献的最佳认可!
编辑 耿超逸










