近日,深圳北京大学香港科技大学医学中心刘伟研究员团队联合南方科技大学刘忠民教授团队及华南理工大学李健潮教授团队,在《自然·通讯》杂志上发表题为“Structural insights into the dual Ca2+-sensor-mediated activation of the PPEF phosphatase family”的研究成果。该研究首次揭示了丝氨酸/苏氨酸蛋白磷酸酶PPEF家族受双重钙离子传感器协同驱动的激活机制,为乳腺癌、胃癌等重大疾病的靶向治疗提供了新的理论依据和潜在干预策略。

作为细胞信号转导的关键调控因子,PPEF家族磷酸酶与乳腺癌、胃癌及遗传性视网膜退行性疾病密切相关。在哺乳动物中,PPEF1在感觉神经元、生殖系统及免疫器官中广泛分布,不仅是乳腺癌发生发展的关键生物标志物,还可作为胃癌mRNA疫苗的潜在靶点;PPEF2则通过调控凋亡信号激酶参与癌症进程,其错义突变与先天性遗传疾病密切相关。然而,与其他磷酸酶家族成员相比,PPEF亚型的结构基础与分子机制长期未明,极大制约了其生物学功能解析及疾病干预策略的开发。
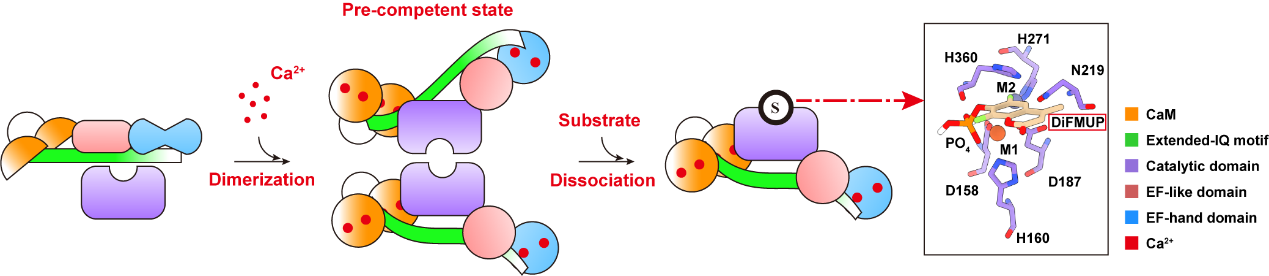
PPEF家族蛋白磷酸酶调控机制示意图。图片由研究团队提供
本研究以PPEF家族的原型成员——果蝇视网膜退化蛋白RDGC为切入点,结合冷冻电镜(Cryo-EM)、X射线晶体学和分子生物学等多学科技术,系统解析了RDGC/钙调蛋白(CaM)全酶复合物在无钙(自抑制态,3.6 Å)和钙结合(激活态,2.8 Å)条件下的高分辨率冷冻电镜结构。
通过冷冻电镜图像和X射线晶体学数据,本研究清晰描绘了PPEF磷酸酶从静息状态到催化位点暴露的动态构象转变过程,揭示了PPEF家族双重钙传感器(CaM和EF-like/EF-hand结构域)协同驱动的“杠杆式”激活机制:在静息状态下,CaM与EF-like/EF-hand结构域协同作用,通过延伸IQ基序(extended-IQ motif)形成“分子锁”,封闭催化位点;钙离子结合后,双重钙传感模块触发延伸 IQ基序发生构象翻转,催化中心暴露,从而实现激活。进一步研究发现,PPEF蛋白磷酸酶受双重钙离子传感器激活的分子机制在进化过程中高度保守,这为在原子层面解析PPEF家族诱发癌症、遗传性疾病的分子病理提供了关键结构框架。
本研究的关键发现包括RDGC/CaM全酶复合物自抑制态结构解析、 RDGC/CaM全酶复合物激活态结构解析、 关键位点突变实验验证、 PPEF家族的功能保守性。本研究的创新之处在于,首次揭示了PPEF家族磷酸酶通过双重钙传感器协同作用驱动延伸IQ基序“杠杆式”翻转的激活机制,为理解丝氨酸/苏氨酸蛋白磷酸酶的动态调控提供了新视角(图1)。同时,通过结构-功能解析锁定关键调控位点,为靶向PPEF介导的疾病(如乳腺癌、胃癌及遗传性神经退行性疾病)提供了潜在的精准干预策略。此外,该研究还为其他钙依赖性磷酸酶的调控机制提供了借鉴,为新型药物开发和信号通路研究奠定了基础。
该论文由刘伟研究员、刘忠民教授和李健潮教授共同担任通讯作者。医学中心博士研究生刘佳与南方科技大学博士研究生吴藏为共同第一作者。医学中心技术员刘宇扬、陈倩苟,硕士研究生丁玉珍,以及上海有机所潘李锋教授、林芷乔和医学中心肖康博士均为本研究做出了重要贡献。冷冻电镜数据的采集与处理得到了南方科技大学高分辨生物电镜结构研究院及冷冻电镜中心的大力支持。本研究获得了国家自然科学基金、广东省自然科学基金及深圳市基础研究基金的资助与支持。
编辑 欧阳晨煜 审读 李斌 二审 党毅浩 三审 王湛