世界卫生组织(WHO)发布的《2022年世界精神卫生报告》数据显示,2019年,全球约有9.7亿人患有精神疾病。该报告认为,COVID-19对人们的精神健康造成了巨大的伤害,在大流行的第一年,抑郁症和焦虑症等常见疾病的发病率增加了25%。
由于精神疾病的病理机制十分复杂,长期以来,人们一直在寻找更加有效的疗法。今年5月,《科学》(Science)杂志刊登了一篇题为“Modulating brain function with microbiota”的文章,作者简·福斯特(Jane A. Foster)认为,肠道微生物及其代谢物可能成为精神疾病治疗的新靶点。
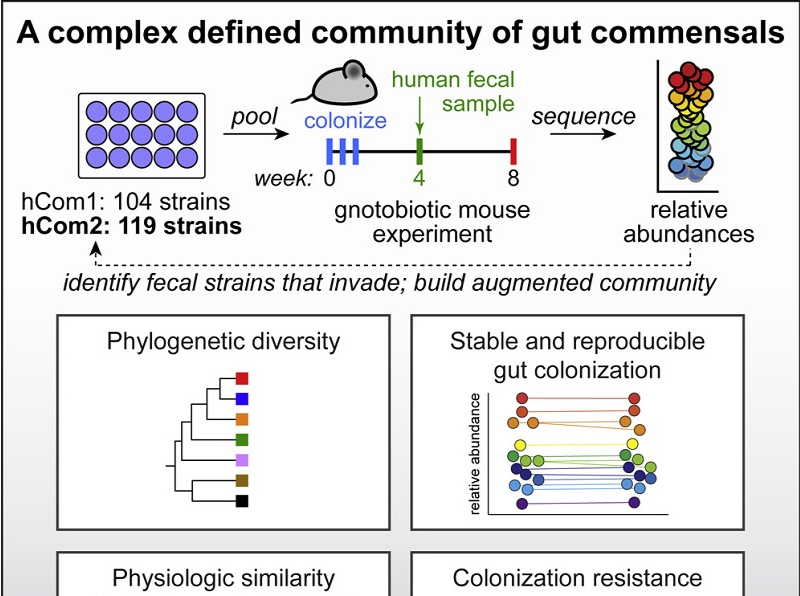
简·福斯特是加拿大麦克马斯特大学(McMaster University)精神病学和行为神经科学系的教授,也是第一个将肠道微生物和“焦虑”联系起来的人。她在文章中表示,肠道菌群—大脑交流在大脑发育、行为和功能中的重要作用已经显现,已经有一些研究者尝试将肌萎缩侧索硬化症 (ALS)和自闭症谱系障碍 (ASD)的临床前发现转化为临床,展现了肠道菌群—大脑交流的潜力。
2021年4月,美国加利福尼亚大学洛杉矶分校(UCLA)综合生物学与生理学系的古丽斯坦·阿吉尔曼(Gulistan Agirman)和伊莱恩· 萧(Elaine Y. Hsiao)曾在《细胞》(Cell)期刊发文,揭示了肠道微生物和大脑之间信号传导的三个通路:免疫、内分泌和系统、神经。
在此背景下,简·福斯特表示,在寻找将肠道微生物群与大脑联系的直接机制的过程中,微生物代谢的潜在作用显而易见。
肠道微生物及其代谢物或可改善ALS症状
以色列魏茨曼科学研究所(Weizmann Institute of Science)免疫学家埃兰·埃利纳夫(Eran Elinav)等人的研究发现,肠道微生物及其代谢物在调节小鼠ALS中具有潜在作用,2019年7月,该研究被发表在《自然》(Nature)杂志上。
在这项研究中,研究人员比较了ALS小鼠和同窝小鼠的肠道细菌,发现了几种可能与ALS相关的微生物,通过微生物移植,鉴定出一个可以使ALS症状好转的微生物物种,以及两个可以使ALS症状恶化的微生物物种。
研究团队猜测,肠道菌群能够影响一种集中于脑的疾病,可能是微生物代谢物造成的。微生物代谢物是指由微生物产生的小分子,它们可以进入血液循环,在全身运行。经过分析,研究团队给容易患上ALS的小鼠注射了烟酰胺(NAM)分子(也称维生素B3),发现小鼠的ALS症状改善。
最后,为了将小鼠实验与人类初步联系起来,该研究团队进行了一项小规模的人类观察实验,收集了37名ALS患者和29名健康人士的粪便样本,对其进行检测,结果显示,ALS患者体内的NAM较少。
这表明,改变ALS患者体内的NAM或可改善ALS症状。但研究团队也指出,他们的人类数据是初步的和观察性的,无法构成对ALS的治疗建议,其中是否蕴含因果机制,还需进行更大规模的研究。
4-EPS影响焦虑的机制被发现,或成为ASD治疗靶点
简·福斯特在《科学》杂志的文章中介绍,“大量临床前和临床证据表明,肠道微生物群在ASD中发挥作用”。早在2013年,美国加州理工学院的萨基斯·马兹曼尼安(Sarkis K. Mazmanian)团队就发现,微生物代谢物 4-乙基苯基硫酸盐 (4-EPS)对 ASD 母体免疫激活小鼠模型和 ASD 个体的行为具有病理生理学影响,但当时未发现其影响机制。
多年后,萨基斯·马兹曼尼安及其团队找到了答案。今年2月,他们撰写的论文 “A gut-derived metabolite alters brain activity and anxiety behaviour in mice”被发表于《自然》杂志。该研究发现,肠道微生物可以将膳食酪氨酸转化为4-EPS,而4-EPS可以通过影响少突胶质细胞和髓鞘形成来影响焦虑样行为。
通过小鼠试验,研究人员观察发现,具有4-EPS的小鼠焦虑水平更高,并且其脑部一些与恐惧和焦虑相关的区域更活跃。观察这些区域的脑细胞,他们发现,少突胶质细胞发生了改变。少突胶质细胞具有十分重要的功能,它可以形成保护神经元和神经纤维的髓鞘。为了确定4-EPS对少突胶质细胞的影响是否有助于改变行为,研究人员使用了一种可以促进少突胶质细胞成熟的药物,结果显示,4-EPS引起的焦虑样行为改变被阻止了。
萨基斯·马兹曼尼安的另一个团队将4-EPS确定为一种可操作的靶点,证明其在临床中的潜力。他们发现一种高表面积球形碳吸附剂AB-2004(也叫做AST-120),它可以经过肠道,吸附相关物质而不被机体吸收。
通过小鼠实验,研究团队首先证明了AB-2004 可以有效降低 4-EPS 的全身水平,并防止 4-EPS 诱导的焦虑样行为。随后,他们在新西兰和澳大利亚开展了开放标签的1b/2a临床试验。试验表明,口服 AB-2004 在青少年ASD患者中安全且耐受性良好,并且可以减少焦虑和易怒。
简·福斯特认为,这项初步观察性试验表明了肠道衍生代谢物在ASD治疗中的潜力。
参考资料:
1. Blacher, E., Bashiardes, S., Shapiro, H. et al. Potential roles of gut microbiome and metabolites in modulating ALS in mice. Nature (2019). DOI:10.1038/s41586-019-1443-5.
2. Gulistan Agirman, Elaine Y. Hsiao, SnapShot: The microbiota-gut-brain axis, Cell(2021).DOI: 10.1016/j.cell.2021.03.022.
3. Jane A. Foster, Modulating brain function with microbiota, Science (2022). DOI: 10.1126/science.abo4220.
4. Needham, B.D., Funabashi, M., Adame, M.D. et al. A gut-derived metabolite alters brain activity and anxiety behaviour in mice. Nature (2022). DOI:10.1038/s41586-022-04396-8.
5. Stewart Campbell, A., Needham, B.D., Meyer, C.R. et al. Safety and target engagement of an oral small-molecule sequestrant in adolescents with autism spectrum disorder: an open-label phase 1b/2a trial. Nature Medicine (2022). DOI:10.1038/s41591-022-01683-9.
(原标题《世界精神卫生日|肠道微生物及其代谢物或成精神疾病治疗新靶点》)
见习编辑 陈桥魁 审读 韩绍俊 审核 关越