在脑机接口等神经接口系统中,电极是连接电子设备和生物神经系统的核心界面传感器,是脑机接口中“接口”的核心所在——然而,当前植入式电极均是“静态”的,植入后只能“固定位置、局限采集”,还在免疫反应中“被动挨打”乃至传导失效,严重制约了脑机接口的应用和未来发展。
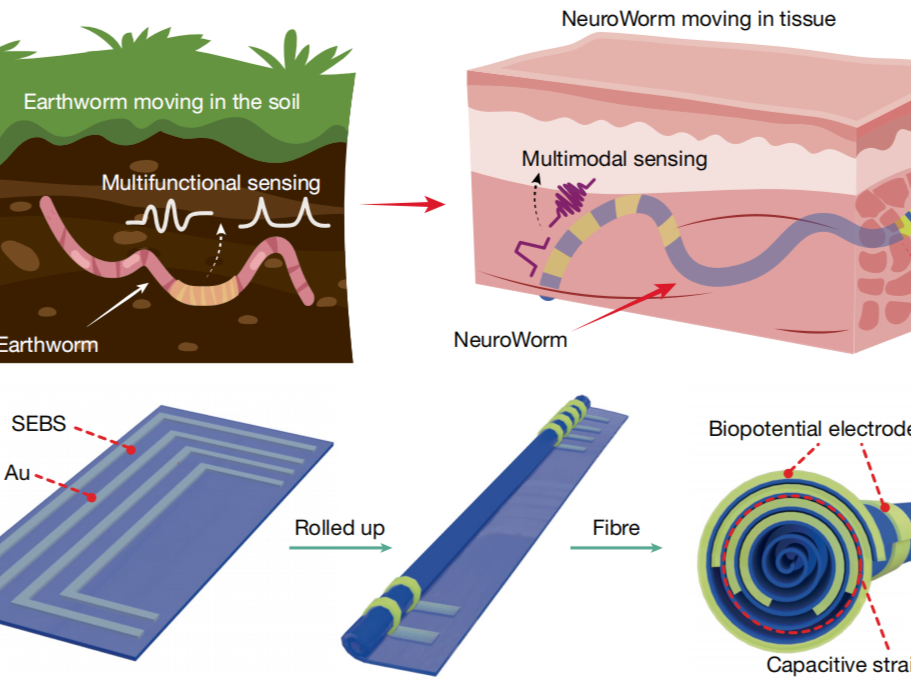
9月17日,由深圳理工大学人工智能研究院特聘教授、中国科学院深圳先进技术研究院(简称“深圳先进院”)刘志远、韩飞团队联合深圳先进院徐天添团队以及东华大学严威团队,历经5年多协同攻关的研究成果在《自然》发表。研究团队成功研发出了如头发丝般纤细、柔软可拉伸、可自由驱动的神经纤维电极——NeuroWorm(神经蠕虫)。该研究首次提出了脑机接口“动态电极”的新范式,打破了植入式电极的“静态”传统,为脑机接口电极的研究与应用开辟了新方向。

论文截图
该研究中,刘志远、徐天添、韩飞、严威为论文共同通讯作者,厦门大学助理教授谢瑞杰(原刘志远团队博士后)与深圳先进院副研究员韩飞、研究助理余潜衡远、博士生李冬为论文共同第一作者。研究工作得到了中国科学院院士郑海荣、中国科学院院士朱美芳以及深圳先进院研究员李光林的帮助与支持。

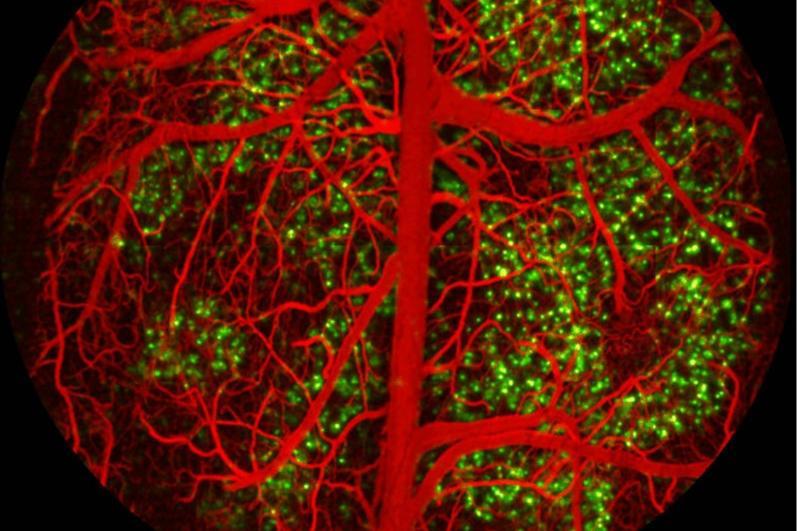
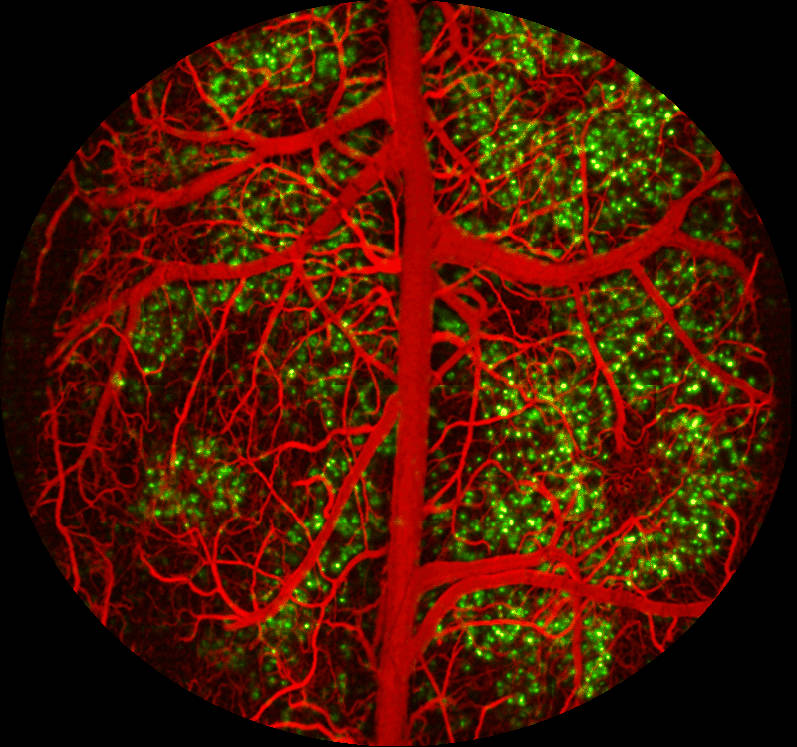
放大镜视野下的60通道神经纤维电极
比头发丝还软,脑机接口迎来“活体”时代
脑机接口分为非植入式、半植入式与全植入式,全植入式脑机接口技术因电极直接与神经元“对话”,可实现其他方式无法企及的监测精度与更丰富的功能。然而,传统植入式电极植入后不仅无法动态调整植入位置,也无法对周边环境作出响应性调整。
“从临床需求来看,如果我们能开发出一种非常细、非常软、又能运动的多通道纤维电极,或许能解决当前电极领域的不足。”在2020年11月一次例会上,刘志远和课题组成员讨论中谈及。
但想要得到这种电极并非易事,不仅要克服多个技术难点,还需要不同领域的工程技术人才。那时,徐天添团队长期专注于磁驱动微型机器人研究,在磁性材料制备及微纳机器人精确操控方面积累了丰富经验。对于传统柔性电极的“静态”特性以及其所导致的问题,刘志远在和徐天添探讨之后,两个课题组一拍即合,决定共同探索如何在柔性电极中引入微小磁性组件,并利用外部磁场实现电极植入后仍具备可调节、可运动的“动态”特性。
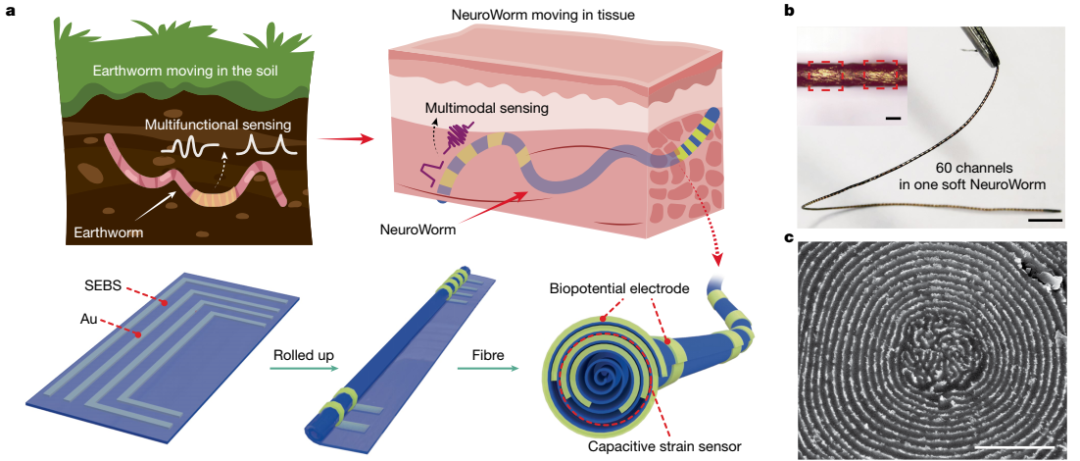
“NeuroWorm”的设计、制造策略和演示
在该研究中,研究团队首先要解决的难题,便是如何在一根直径约为200微米的纤维上,布局数十个独立的电极通道,这相当于在一根头发丝上拆分雕刻出数十根长度一致、彼此不能交叉的细线,还要保证这根纤维足够柔软且可拉伸。
团队成员谢瑞杰此前制备出了厚度仅为数百纳米厚的超薄薄膜电极,在此基础上,他想到如果将薄膜“卷起来”,就能变成微米尺度的纤维。通过超薄柔性薄膜的制备、导电图案设计、软硬接口设计和制造等多个精细步骤,经过五年攻关,研究团队在郑海荣院士、李光林研究员的帮助下,终于制备出拥有沿着纤维长度方向独立分布的多达60个通道的、直径仅有196微米的柔软可拉伸纤维电极。
为了让制备的电极“动起来”,团队在电极的一端增加了微小的磁头,通过结合高精度磁控系统和即时影像追踪技术,使电极能够在体内自主调控前进方向,并能稳定记录高质量的生物电信号。这样的“动态电极”可以在兔子颅内“游走”,根据需要主动更换监测目标,研究团队给它命名为NeuroWorm——神经蠕虫。
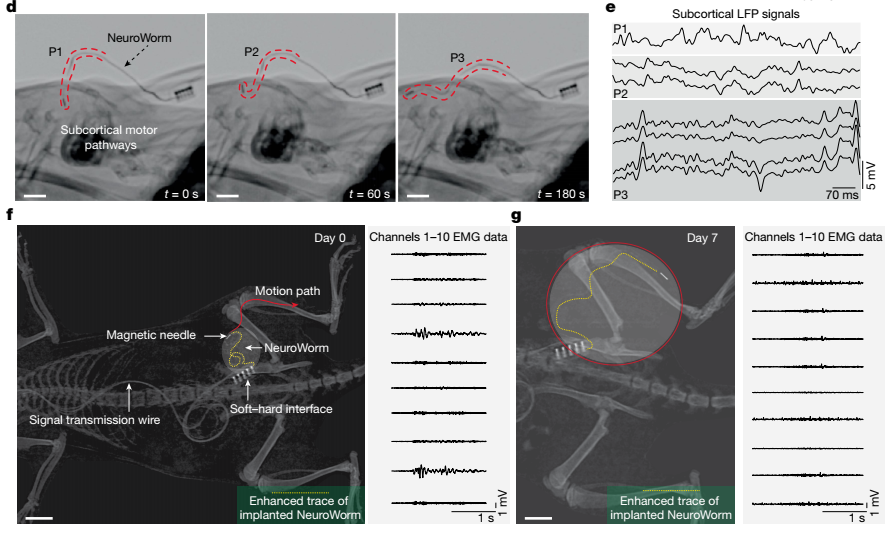
磁场控制下“NeuroWorm”对脑部与骨骼肌的动态监测
开创智能响应机制,跟着磁场主动“遛弯”换位置
NeuroWorm的诞生不仅为脑机接口开辟了新路径,它的应用还远不止于大脑。研究团队还首次实现了电极在肌肉内的长期植入与稳定工作。
与大脑相比,外周肌肉在运动过程中会产生更大幅度的形变和拉伸,对电极的柔软性、耐久性和信号稳定性提出了更高要求。NeuroWorm凭借其微型化、可拉伸的结构优势,在肌肉内依然能紧密贴合组织,并保持高质量信号采集,为外骨骼控制、康复辅助以及日常环境中的人机协同提供了新可能。
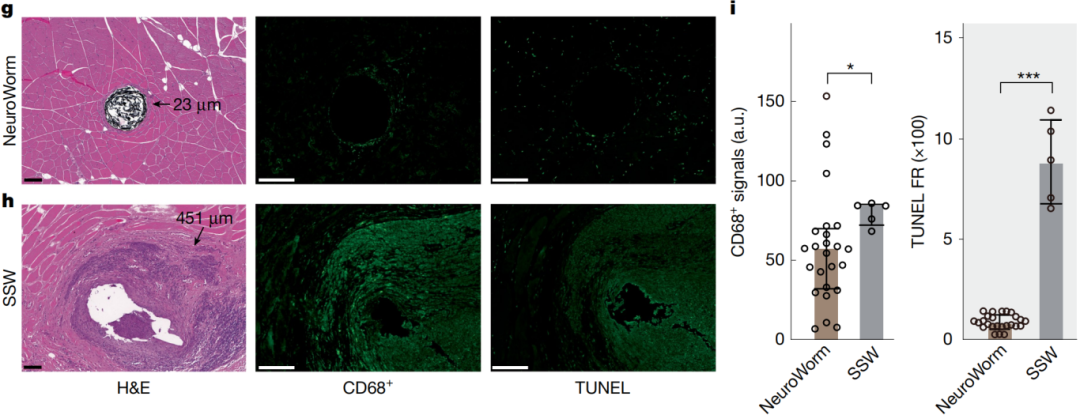
NeuroWorm肌肉束内长期植入生物相容性验证
团队利用微创植入技术,成功实现了NeuroWorm电极在大鼠腿部肌肉内稳定工作超过43周。值得关注的是,电极植入13个月后,其周围形成的纤维包裹层厚度平均不足23微米,周围组织的细胞凋亡率与正常组织相当,展现了优异的长期生物相容性。相比之下,传统不锈钢丝电极在相同条件下包裹层厚度超过451微米,伴随显著的细胞凋亡反应。
与此同时,在外部磁场的操控下,NeuroWorm可在肌肉上表面实现游走,可在植入后的一周内每天变换位置进行监测。
“研究过程中,我们不仅要确保电极信号传输的稳定性、防水性,还要确保精准控制电极在实验动物体内运动。在很长的一段时间里,我们的大部分工作是不断地改进、调整、动物实验测试,最终得到符合要求的电极。”韩飞回忆。
“这一成果标志着生物电子学领域的重要突破,使传统的被动固定式植入电极首次迈向可主动控制、智能响应、与生物组织协同运动的全新阶段,为神经系统功能的长期动态监测提供了全新的技术路径。”徐天添表示。
跨学科破壁,有望应用于早期植入式医疗设备中
近年来,随着人工智能、神经生物学、生物传感器与柔性电子等技术不断突破,脑机接口技术已不再依赖单一学科的驱动,更需要AI、材料科学、电子工程、神经科学等多学科的深度融合与协同合作。


率先取得医疗器械注检认证的柔性可拉伸电子皮肤
此前,刘志远团队基于柔软可拉伸导电材料的技术积累,率先实现了柔软可拉伸电极阵列的工程化量产,并通过了相关的二类医疗器械注检,应用在体表高密度肌电监测与刺激等场景中,尝试取代传统的硬质不可拉伸电极阵列,并已实现对包括欧洲客户在内的电生理公司供货。
“尽管我们取得了一些应用突破,又新提出了‘神经蠕虫’的理念,但电极植入后仍面临免疫排异和长期稳定工作等挑战。如何实现电极与人体组织的更好融合,提高信号读取的精准度和稳定性,是未来的重要研究方向。”刘志远表示,未来植入式电极还需在驱动方式、速度控制、材料优化、功能集成、长期相容性等方面开展研究,需要全球科学家的共同努力。
徐天添介绍,研究团队首次将磁控驱动技术运用在植入式电极中,也为磁控微纳机器人领域带来宝贵的经验和数据,有望应用于早期的植入式医疗设备中,为动态监测生理信号提供新的解决方案。

共同通讯作者刘志远(右一)、徐天添(左一)、韩飞(右二),共同第一作者谢瑞杰(左三)、韩飞、余潜衡远(右三)、李冬(左二)
据了解,该研究有望为纤维器件的制备提供新思路,也为脑科学研究、神经调控、脑机接口、人机协同等领域提供新的工具。未来,研究团队还将继续在动态柔性电极和“活性”主动响应型柔性电极领域进行深入研究,推动脑机接口技术的发展进程。
(受访单位供图)
编辑 刘彦 审读 吴剑林 二审 王雯 三审 潘未末