4月17日,国际顶级学术期刊《自然》(《Nature》)报道了南方科技大学化学系副教授田瑞军团队与美国Salk研究所Tony Hunter院士团队针对胰腺癌的功能蛋白质组学研究工作。这一中美合作的科研成果意义重大,在发现以及治疗“癌症之王”胰腺癌方面有重大突破,随着这项科学研究未来进入应用阶段,有望为全球胰腺癌患者带去生命的曙光。

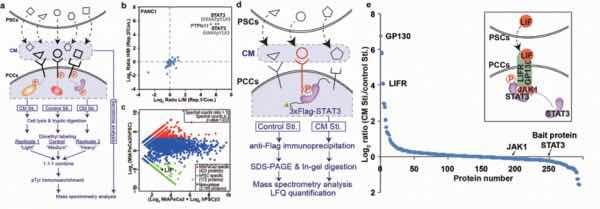
整合蛋白质组学分析策略及白血病抑制因子LIF的发现
整合蛋白质组学助力攻克“癌症之王”难题
该研究成果以“Targeting LIF-mediated paracrine interaction for pancreatic cancer therapy and monitoring”为题在Nature发表。田瑞军为文章的共同通讯作者。化学系博士后高伟娜、首届博士生黄培武和化学系博士后袁枭分别为文章的并列第二、第四和第五作者。南方科技大学第一附属医院癌症研究所所长许瑞莲为本文的共同作者。
田瑞军告诉记者,胰腺癌是恶性程度最高的肿瘤之一,而且近年来发病率在我国呈上升趋势。此前对于胰腺癌的诊断缺乏有效手段,既没有有效的靶向药,也没有有效的标志物可辨认,通常被确诊时已经进入中晚期,且大部分已发生转移扩散。最低的存活率和极短的生存期使其被称为“癌症之王”。
众所周知,苹果的创始人乔布斯就是由于胰腺癌去世,田瑞军表示,乔布斯的儿子也十分关注他们这项研究,还曾经与他们在美国的研究团队交流,表示对这项研究的支持。
针对胰腺癌的诊断及治疗难题,八年前,美国Salk研究所Tony Hunter院士团队找到田瑞军团队共同合作研究。经过漫长的研究,他们发现了介导胰腺癌细胞和星状细胞之间信号转导的关键因子白血病抑制因子(Leukemia inhibitory factor, LIF),并系统地验证了其作为胰腺癌治疗靶点和生物标志物的可行性。“通过在血液中对LIF的检测,我们可以有效地区分正常人、胰腺癌病人及不同阶段的胰腺癌病人。”田瑞军介绍。

中美多中心、多检测手段验证LIF为胰腺癌生物标志物
研究者首先开发了应用于研究肿瘤微环境中细胞间信号转导的整合蛋白质组学分析策略,发现了转录因子STAT3的磷酸化激活是癌细胞内最显著的分子变化,而星状细胞分泌的LIF是导致这一分子事件的最关键旁分泌因子。
通过采用多中心(中国和美国)和多种类型检测手段(靶向性质谱和高灵敏度ELISA)相结合的方式,研究者对大量临床组织样品的定量分析发现LIF在胰腺肿瘤组织中特异性高表达,并且与其他常见实体瘤相比,LIF的癌特异性高表达具有明显的胰腺癌特异性。相关性分析表明,LIF在胰腺肿瘤组织中的表达量与病人的病理状况,特别是分化状态及生存期紧密相关。同时,病人血液中的LIF变化水平与药理反应的病理分析结果高度一致,由此证明其作为胰腺癌生物标志物的可行性。
在实现对胰腺癌的诊断之外,他们还发现,LIF蛋白是一个治疗胰腺癌的全新的药物靶点。由于晚期胰腺癌对化疗药物有很强的耐受性,而且对放射治疗不敏感,目前胰腺癌的治疗效果都难尽如人意。而LIF蛋白的发现,将有望破解胰腺癌的治疗困境,为胰腺癌病人带去生存的希望。
中美科学家越洋合作完成课题
田瑞军告诉记者,在《自然》发表文章后,他们的研究并未结束。目前,他们正在与武汉同济医院、深圳市人民医院(南科大第一附属医院)等合作开展研究,希望能够进一步证明LIF能够在患病的早期阶段就对其进行诊断。而靶向LIF的单克隆抗体药物的临床实验也正在准备阶段。
而在北美,这项工作则进展得更加迅速。基于他们发现的LIF在胰腺癌中的关键性作用,加拿大Northern Biologics公司去年将胰腺癌纳入其anti-LIF抗体的I期临床试验中,并将胰腺癌作为重点适用病症进行测试。
此次与田瑞军开展合作的美国Salk研究所Tony Hunter教授是美国科学院院士,曾被预测为诺贝尔奖热门获奖人选。他是癌症研究领域的顶尖学者,研究成果引导超过了10种重要抗癌药物的发现,其中包括著名抗癌药物格列卫。对于此次成果的发表,他也十分兴奋。Hunter教授表示,这是他50多年科研生涯中所领导的最接近临床转化应用的一项研究,在短短数年间完成了从最初的盲筛到I期临床试验的开展。
田瑞军表示,Tony Hunter教授之所以找他的团队合作,正是看中了他们在生物质谱与蛋白质组学技术方面的高水平研究和南科大高端的生物质谱平台,从而达成了这次中美的越洋合作。近年来,田瑞军课题组开发了一系列新的生物质谱和蛋白质组学分析新策略,并在创新药物发现、癌症靶点和标志物开发、肠道微菌群宏蛋白质组分析和干细胞蛋白质组分析等方面实现了系统地应用。田瑞军期待团队开发的生物质谱和蛋白质组学技术能够为粤港澳大湾区重点推进的生物医药研究做出更大的贡献。
【读特新闻+】
南科大蒋伟课题组成果登上顶级期刊
格拉布斯研究院大分子材料中心双聘教授、南科大化学系教授蒋伟课题组近日制备了一种具有高度可拉伸性能的瞬态(耗散)水凝胶。该研究成果发表在化学领域顶级期刊《Nature Chemistry》上。南方科技大学深圳格拉布斯研究院和化学系是该项研究的通讯单位,蒋伟为唯一通讯作者。
蒋伟课题组在过去六年的时间里,通过模拟生物受体的空腔特征,合成了一系列具有独特结构特征的大环主体分子,实现了生物分子识别和自组装的仿生模拟。在近期的研究中,蒋伟课题组发现酰胺内修饰分子管能够穿到聚乙二醇的高分子链上,形成一个像项链一样的多聚假轮烷结构。每个分子管具有四个羧酸根,能够与金属离子配位。当加入铜离子时,多聚假轮烷就会通过链间配位交联,形成一个不能自由流动的水凝胶结构。
该瞬态水凝胶具有非常优异的拉伸性能,至少能被拉伸至其初始长度的30倍。在拉伸过程中,分子管能够在聚乙二醇高分子链上“摩擦”滑动。这种“分子滑轮”结构有利于耗散拉伸应力,故而展现出较好的拉伸性能。此外,该水凝胶还可以在摇动条件下实现快速自修复。该研究为构建耗散自组装材料提供了新的思路,在智能材料领域具有潜在的应用前景。
南方科技大学深圳格拉布斯研究院是以小分子催化和大分子材料为核心科研领域的研究机构。该成果是深圳格拉布斯研究院大分子材料中心2019年伊始所取得重大科研成就之一。随着研究院科研平台和科研团队建设的进一步完善,以及研究院与化学系等其他兄弟院系深入合作的展开,研究院将进一步提升催化化学、高分子材料化学及交叉学科的科研能力,涌现更多的科研成果。
编辑 张克